Задача: Где больше молекул: в комнате объемом 50 м3 при нормальном атмосферном давлении и температуре 20 °С или в стакане воды объемом 200 см3?
Пояснение: Обозначим: V1 объем комнаты, p — давление воздуха, t — температуру воздуха в комнате по шкале Цельсия, T — абсолютную температуру воздуха, т.е. его температуру по шкале Кельвина, V2 — объем воды в стакане, N1 — число молекул воздуха в комнате, N2 — число молекул воды в стакане, k — постоянную Больцмана, m — массу воды в стакане, m0 — массу молекулы воды, ρ — плотность воды, M — молярную массу воды, NA — число Авогадро.

Здесь Т = t + 273 = 20 + 273 = = 293 К.
Поскольку теперь все величины в формуле (1) известны, вычислим N1:
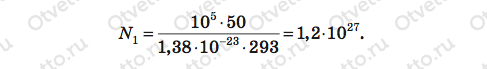
Число молекул воды N2 можно найти, разделив массу воды в стакане m на массу одной молекулы m0:
N2 = m/m0. (2)
Массу всей воды в стакане найдем, умножив ее плотность ρ, т.е. массу каждой единицы объема воды, на объем воды V2:
m = ρ · V2. (3)
Выразим объем воды в единицах СИ:
200 см3 = 200 · 10–6 м3 = 2 · 10–4 м3.
Массу одной молекулы воды m0 найдем, разделив молярную массу воды М, т.е. массу всех молекул в одном моле воды, на их число в нем, т.е. на число Авогадро NA:

Сравнив численные величины N1 и N2, мы увидим, что число молекул воздуха в комнате больше, чем число молекул воды в стакане.
Ответ: N1 = 1,2 · 1027, N2 = 6,7 · 1022, в комнате молекул воздуха больше, чем молекул в стакане воды.
