Задача: В баллоне находится газ при температуре 15°С. Во сколько раз уменьшится давление газа, если 40 % его выйдет из баллона, а температура при этом понизится на 8°С?
Пояснение: Обозначим t начальную температуру газа по шкале Цельсия, T — эту же температуру по шкале Кельвина (абсолютную температуру), ∆T — изменение температуры, m — начальную массу газа, ∆m — изменение массы газа в баллоне (или массу газа, вышедшего из баллона), V — объем газа, R — молярную газовую постоянную, M — молярную массу газа, р1 — начальное давление газа в баллоне, р2 — его конечное давление.
Указание: изменение температуры по шкале Цельсия ∆t равно изменению температуры по шкале Кельвина ∆Т, т.е. если ∆t = 8 °С, то и ∆Т = 8 К.

После того как из баллона вышла масса газа ∆m, в нем осталась масса m – ∆m , и при этом температура газа понизилась на ∆Т, т.е. стала равной Т – ∆Т. Поэтому теперь запишем уравнение Менделеева — Клапейрона для нового состояния:

Выразим начальную температуру в единицах СИ: 15 °С = 288 К.
Произведем вычисления:
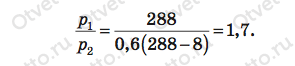
Ответ: р1/р2 = 1,7.
